海外医療機器メーカーの
薬事申請・日本市場展開のワンストップ支援

日本市場への参入をご検討中のメーカー様
貴社の製品は日本国内承認を取得されていますか?
- CE・FDA取得済み製品のPMDA移行に特化
- 外国製造業者登録から国内販売体制までサポート
- 柔軟な契約形態と成果報酬型も導入可能
日本国外機器メーカーの日本への進出において、最も大きな障壁のひとつが日本国の「薬機法(PMDA・認証機関)に基づく承認・認証取得」です。
日本の薬事申請は、他国と比べて要求される文書や審査プロセスが極めて厳格であり、現地の専門家による対応が不可欠と言えます。
MedRegi(メドレジ)は、海外メーカー様が日本市場に参入するために必要な薬機申請業務をトータルでサポートする、日本国内でも数少ない専門サービスです。
Benefits -Why MedRegi-
MedRegi申請が選ばれる理由
PMDA申請の移行
すでにCEやFDAなどの国際的な認証取得済みの製品について、日本向けにスムーズな申請準備・提出を支援
外国製造業者の申請登録
外国企業単独では難しい申請スキームやQMS適合性調査の対応も含めてご支援
柔軟な契約形態と成果報酬型
初期費用を抑え、成果ベースでのご支援に対応
Coverage -Diverse Fields-
多様な医療分野に対応
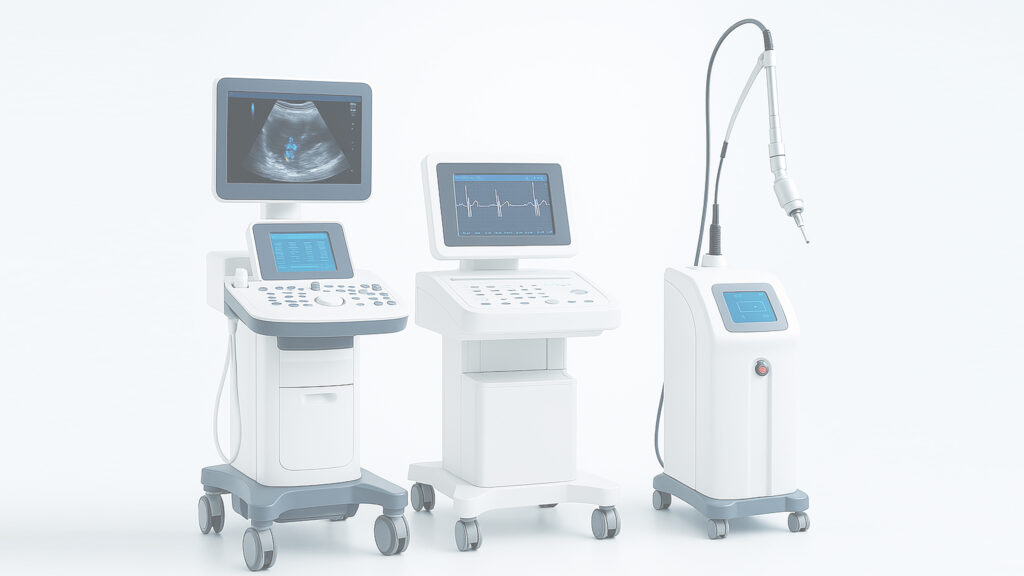
MedRegiでは、美容医療機器のみならず、以下のような幅広い製品分野を対象に申請支援を行っております。
- 一般医療機器(画像診断、治療機器など)
- 体外診断用医薬品(IVD)
- PMDA・認証機関との交渉力
- 迅速な対応と手厚いサポート
Aftercare -PostMarket Support-
許認可後の日本市場での展開もサポート

許認可後の市場展開もお任せください。
MedRegiでは、申請支援にとどまらず、承認・認証取得後の国内展開支援(販売先開拓・パートナー企業のマッチングなど)も行っております。
「申請後にどう販売していくか」まで視野に入れ、貴社製品の日本市場での定着をゴールとした伴走型サポートを提供しています。
Contact Us
お問い合わせ
online interviews
オンライン面談から対応
MedRegiでは、海外医療機器メーカー様向けに、日本市場への薬機法申請に関するご相談を、オンライン商談形式で承っております。
PMDA(医薬品医療機器総合機構)や日本国内の認証機関との申請手続きに精通した専門チームが、申請までのステップや必要書類、日本特有の制度に関する留意点などを丁寧にご説明いたします。
「CEマークやFDA承認は取得済みだが、日本への申請が初めて」「代理店を持たずに日本市場に展開したい」といったニーズをお持ちの企業様も安心してご相談ください。
まずはお気軽に、オンラインにて面談をお申し込みいただき、貴社製品の特性や現状やご希望に合わせた最適な申請方針や支援内容をご案内させていただきます。
グローバル動向と日本制度の両面に精通した担当者が、貴社の日本進出をサポートいたします。